서론
메니에르병은 수분에서 수시간 지속되는 어지럼이 발작성, 반복성으로 나타나면서 청력저하, 이명, 이충만감 등의 귀 증상을 동반하는 질환이다. 반복적인 어지럼증을 유발하는 흔한 원인질환 중 하나로서, 치료가 제대로 이루어지지 않으면 삶의 질 저하 및 그로 인한 우울, 불안감 등을 유발할 수 있다.
메니에르병의 발생기전은 명확히 밝혀지지 않았으며, 여러 가설에 기반하여 메니에르병의 치료를 위한 여러 약제가 소개되었다. 고실 내 스테로이드 주입술(intratympanic steroid injection, ITSI)은 돌발성 난청환자에서 스테로이드의 전신적 부작용은 줄이면서 면역억제 효과를 활용하기 위한 치료로 제시되어 왔다. 최근 메니에르병에서 고실 내 스테로이드 주입술에 대한 논의가 많이 이루어지고 있으며, 치료 방법 및 효용성이 매우 다양하게 보고되고 있다. 본론에서는 관련된 문헌 고찰을 통하여 고실 내 스테로이드 치료법의 효용성을 확인하고, 임상에서의 적용가능성을 알아보고자 한다.
본론
메니에르병의 유병률은 2010년 미국 연구에서는 10만 명당 대략 3.5-513명 정도,1) 2005년 일본 연구에서는 10만 명당 연평균 34.5명 정도로 매우 다양하게 보고되었다.2) 최근 보고된 한국에서의 유병률은 10만 명당 35.8-153명 정도로 해가 갈수록 증가하는 형태를 보였고, 고령층과 여성에서 더 많이 확인되었다.3) 한국 사회의 고령화가 점점 더 진행되어 간다는 점을 고려할 때, 메니에르병의 유병률과 사회적 의미 또한 함께 증가할 것으로 예상된다.
메니에르병은 특징적으로 나타나는 반복적인 어지럼증, 그리고 어지럼과 동반되는 귀 증상(청력저하, 이충만감, 이명 등)을 호소하는 환자에서 의심해볼 수 있다. 1995년에 AAO-HNS(the American Academy of Otorhinolaryngology-Head and Neck Surgery)에서 메니에르병의 진단기준을 제시하였으며, 이후 Barany Society, 미국, 유럽, 일본, 한국이 함께한 분류 위원회에 의해 메니에르병에 대한 진단기준이 공동으로 공식화되었다(Table 1).4) 이 기준에 따라 이전에 메니에르병, 메니에르증후군, 내림프수종 등으로 불리던 용어들을 통일하고, 특징적인 어지럼증의 지속시간이나 귀 증상의 양상 등에 따라 확실한 메니에르병(Definite MD)과 가능성이 높은 메니에르병(Probable MD)으로 분류하였다.
| 가능성 높은 메니에르병(probable Meniere’s disease) |
|---|
| A. 20분 – 24시간 지속되는 회전성 어지럼 혹은 현기증이 2회 이상 발생 |
| C. 이환측 귀에서 변동성의 청각증상(난청, 이명이나 이충만감)이 동반된 경우 |
| D. 다른 원인은 배제되어야 한다. |
Paparella의 2008년 논문에서는 메니에르병의 치료를 위한 알고리즘을 제시하였다.5) 메니에르병으로 진단된 모든 환자에서 생활습관 개선을 교육한 뒤, 3-6개월간 먼저 이뇨제, 스테로이드(경구 복용, 근육 내/고실 내 주입) 등을 시도해보고, 이후 치료경과에 따라 침습적 치료(고실 내 겐타마이신 주입술, 내림프낭 수술, 전정신경절제술 등)를 고려한다.
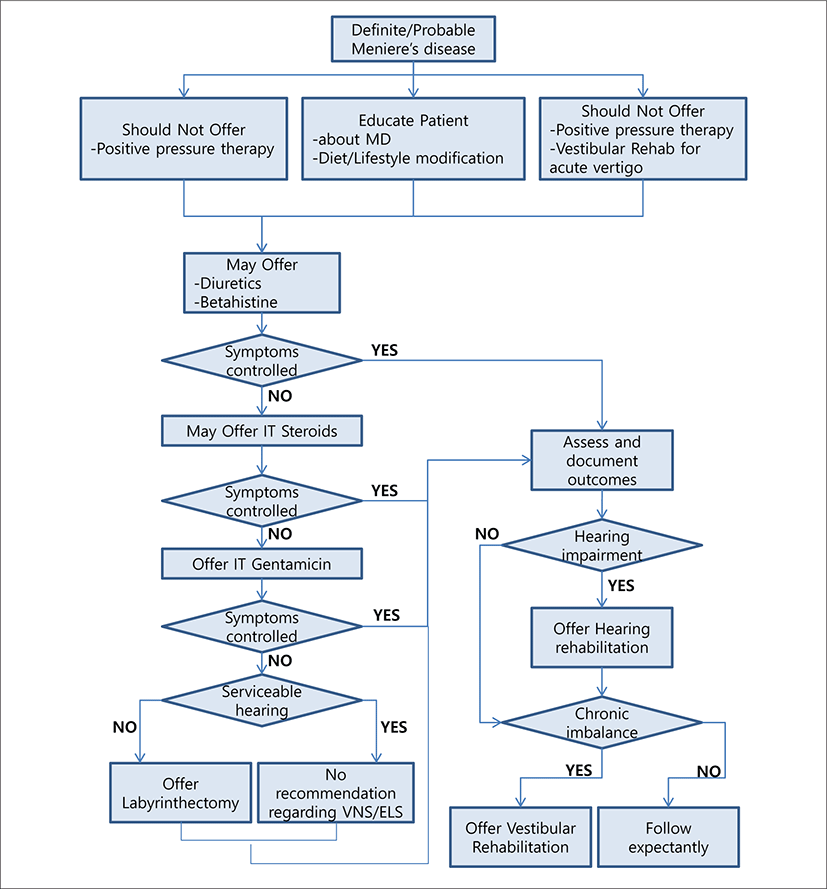
최근(2020년) 미국의 연구결과를 기반으로 메니에르병의 임상적 가이드라인이 제시되었다(Fig. 1).6) 여기에서는 메니에르병의 치료를 위하여 기존에 사용되는 여러 방법들을 크게 4개 카테고리(강력히 추천-추천-선택적 사용-반대)로 분류하였다. 어지럼 증상 조절을 위한 전정 억제제의 제한적 사용, 증상 경감과 예방을 위한 식습관이나 생활습관 교육은 ‘추천’되며, 이뇨제나 betahistine과 같은 유지 약물치료는 ‘선택적 사용’으로 분류되었다. 고실 내 스테로이드 주입술은 보존적 치료에 반응하지 않는 활동성 메니에르병에서 ‘선택적 사용’으로 분류되었고, 고실 내 겐타마이신 주입술은 비절제 치료에 반응하지 않는 활동성 메니에르병에서 ‘추천’으로 분류되었다. 이러한 비수술적 치료에도 반응하지 않는 메니에르병에서, 수술적 치료(labyrinthectomy 등), 전정재활치료, 상담치료는 ‘추천’되며, 급성 현훈 발작이 있는 메니에르병에서 전정재활치료는 ‘반대’로 분류되었다.
유럽에서 2018년 발표한 성명에서,7) 메니에르병의 1차 치료는 예방을 위한 개인화된 접근으로서, 메니에르병의 원인이 되는 동반 병증을 치료하고 식습관을 개선하며, diuretics나 betahistine과 같은 유지 약물치료를 제시하였다. 이러한 1차 치료에도 반응하지 않으면 2차 치료로 고실 내 스테로이드 주입술을 고려해 볼 수 있다.8,9) 그럼에도 반응하지 않는 경우, 3차 치료로 수술적 치료(endolymphatic sac surgery, dexamethasone injection into the sac), 4차 치료로 고실 내 겐타마이신 주입술, 5차 치료로 보다 침습적인 수술(labyrinthectomy, vestibular neurectomy)을 고려해볼 수 있다.
내이질환에서 스테로이드는 cellular edema의 완화나 membrane stabilization과 같은 진정작용을 나타낼 것을 기대하며 사용되었다.10) 고실 내로 주입한 스테로이드는 주로 정원창(round window)을 통해 내이의 고실계(scala tympani)로 전달된 후 나선 인대(spiral ligament)와 Rosenthal’s canal을 통해 수분 이내에 빠르게 전정계(scala vestibule)에 도달하며, 이후 고실계와 코르티 기관(organ of Corti), 나선신경절(spiral ganglion)의 소통 경로를 통해 유모세포와 신경세포로 전달된다.11) 이렇게 스테로이드가 내이로 전달되는 과정에는 약물 분자의 무게, 농도, 양과 같은 외인성 요인부터, 정원창의 상태나 외림프 흐름의 패턴과 같은 내인성 요인이 영향을 미칠 수 있다.12)
내이로 전달된 스테로이드의 작용기전은 아직 명확히 밝혀지지 않았으며, 크게 두 가지 기전을 통해 효과를 보이는 것으로 추측된다. 첫째는 면역억제 작용으로, 중이염13)이나 소음,14) 허혈15) 등의 원인으로 인한 와우의 초기 염증과정이 모두 스테로이드에 반응한다고 보고되었다. 두번째는 이온 항상성 유지 작용이다.16) 청각 및 전정 유모세포의 기능에 필요한 내림프액 전위의 유지에 칼륨 이온 및 수분의 순환이 매우 중요하다. 스테로이드는 염증과정에서 이러한 이온채널이나 aquaporin 등을 손상시키는 염증전구물질의 발현을 억제함으로써 간접적으로 이온항상성 유지에 관여하기도 하고,17,18) 직접적으로는 mineralocorticoid receptor나 glucocorticoid receptor에 결합해서 이온채널 합성유전자의 발현을 유도하기도 한다.19)
앞서 언급한 여러 기전을 통한 효과를 기대하며 스테로이드를 내이질환의 치료에 적용시켜 볼 수 있으며, 그러한 질환에는 자가면역질환 이외에도 특발성 돌발성 난청이나 메니에르병이 포함된다.
메니에르병을 가진 환자에게 고실 내 스테로이드 주입술을 적용하는 것은 1987년 Sakata group에 의해 처음 기술되었다.20) 스테로이드의 전신 투여와 고실 내 주입술을 통한 국소 투여가 내이로의 약물전달에 차이가 있는지를 연구한 연구에서, 고실 내 주입술이 전신 투여에 비해 더 높은 내이 전달율을 보였으며,21) 그럼에도 혈장내 농도는 낮게 측정되었다.22,23) 이에 따라 스테로이드의 효과를 높이고, 전신적 부작용을 줄이는 방법으로 고실 내 스테로이드 주입술을 고려해볼 수 있다.
고실 내 스테로이드 주입술의 효용에 대해서는 현재까지 많은 연구가 이루어졌으나, 사용한 약제의 종류나 용량, 주입방법, 주입 시기, 연구 디자인과 대상 환자 수 및 조사방법 등의 다양성으로 인해 매우 다양한 결과가 보고되었다.24) 그 결과, 현재 고실 내 스테로이드 주입술은 메니에르병의 치료를 위한 최우선 방법으로는 추천되지 않으나, 최우선적으로 시행하는 증상조절 및 유지약물치료, 생활습관 개선에도 증상이 호전되지 않는 경우 구제적 목적으로 고려해볼 수 있는 방법으로 여겨진다.6,7,25-27)
Placebo그룹과의 대조군 연구에서, 고실 내 겐타마이신 주입술은 어지럼 증상의 조절에 효과적이라고 보고된 바 있고, 청력 저하 합병증에 대해서는 의견이 분분하다.28) 고실 내 주입시 스테로이드(dexamethasone)가 겐타마이신에 비해 어지럼 증상 조절 효과가 떨어지며, 청력에서는 뚜렷한 차이를 보이지 않는다고 보고한 연구29)가 있다. 그러나 메니에르병의 고실 내 약물 주입술에 대한 여러 비교연구에서 스테로이드는 겐타마이신과 큰 차이를 보이지 않는다고 제시한 경우들도 있다.30,31) 메니에르병에서 고실 내 주입술에 사용되는 약물에 따른 치료효과를 메타분석을 통해 비교한 연구에서는, 모든 약제가 placebo와 유의미한 차이를 보였다.32) 그 중에서도 gentamicin이 가장 효과적이었고, 다음으로 methylprednisolone, latanoprost(prostaglandin analogue), dexamethasone, ganciclovir 순으로 효과를 보였다.
고실 내로 겐타마이신을 주입한 쪽에 전정 및 청각 손상이 발생할 드문 가능성28)과 메니에르병 환자가 양측성으로 진행할 가능성33), 장기간 경과 관찰한 결과, 스테로이드와 겐타마이신의 효과가 큰 차이를 보이지 않는 점32,34) 등을 고려할 때, 고실 내 스테로이드 주입술을 우선하여 시행해 볼 수 있고, 이후 경과관찰하면서 환자의 어지럼 증상 및 심각도, 청력에 따라 고실 내 겐타마이신 주입술까지를 순차적으로 고려할 수 있겠다.
고실 내 주입술에 적용 가능한 스테로이드에는 여러 종류가 있다. 중이 공간으로 주입한 스테로이드가 내이로 흡수되고 작용하는 과정에서 스테로이드 약제에 따른 어떠한 차이가 있는지 명확히 밝혀진 바는 없다. 약제에 따라 서로 다른 무기질코르티코이드(mineralocorticoid) 및 당질코르티코이드(glucocorticoid) 특성을 가지며, 분자구조에 따라 서로 다른 화학적 특성(pH, osmolarity 등)을 가지므로, 같은 농도에서도 서로 다른 전달율 및 유지 시간을 보일 수 있다. 그러므로, 고실 내 스테로이드 주입술에서 스테로이드 약제에 따른 차이에 대해서는 동물 실험결과와 여러 임상연구의 결과들을 통해 추론해 보아야 한다.
단, 스테로이드는 약제에 따라 비슷한 상품명을 가졌으나 분자구조나 특성의 차이가 크거나, 이름은 달라도 분자구조가 유사한 경우가 있다. 그러나 이런 약제별 nomenclature가 잘못 쓰여진 연구들이 많아, 연구결과를 확인하고 비교함에 있어 주의가 필요하다.35) 뿐만 아니라, 스테로이드는 약제에 따라 각기 다른 역가(potency)를 가지며, 이는 약물의 투여경로 및 방법에 따라서 달라질 수 있으므로 이에 대한 고려 또한 필요하다. 경구 혹은 정맥투여를 기준으로 역가를 계산해 보면, dexamethasone 5 mg은 methylprednisolone이나 triamcinolone 약 26.7 mg에 해당한다.
Parnes 등의 내이 스테로이드 약동학에 대한 동물 연구에서, dexamethasone이나 hydrocortisone에 비해 내이에서 더 높은 농도로 흡수되어 오래 유지되는 methylprednisolone이 치료효과가 더 뛰어나다고 보고했다.21-23) Trune 등의 동물연구에서는 methylprednisolone이 dexamethasone에 비해 Mineralocorticoid receptor에 더 큰 친화성을 가진다고 보고하기도 하였다.18) 반대로, 이렇게 내림프에서 dexamethasone의 농도가 낮은 것은 세포 내 dexamethasone의 농도가 더 높다는 것을 의미하므로 methylprednisolone보다 치료효과는 더 뛰어날 것이라고 말하는 연구도 있다.16,36) Triamcinolone과 triamcinolone-acetonide, dexamethasone의 세가지 약제에 대해 내이 약동학을 연구한 논문에서는, 세 약제를 모두 현탁액 형태로 통일하여 기니피그의 중이 내로 주입하고, 외림프로의 흡수 및 제거를 확인하였다.37) 그 결과, triamcinolone은 triamcinolone-acetonide보다 외림프로의 흡수속도는 느렸으나 농도는 유사하게 전달되었고, 제거 또한 triamcinolone-acetonide나 dexamethasone보다 느려 외림프 내에 더 오래 유지되었다. 그러므로, 약제의 형태와 무관하게 triamcinolone이 다른 약제에 비해 와우의 정점부(apex)까지 효과적으로 전달될 가능성을 보여준다.
실제로 메니에르병 환자에게 고실 내 스테로이드 주입술을 시행한 연구들(Table 2)에서, 어떤 스테로이드약제를 어떤 농도, 어떤 용량으로 주입할지에 대한 기준은 명시되어 있지 않다.30,38-41)
| 참고논문 No. | 연구 | 대상 | 치료약제 | 주입 횟수 | 주입 간격 | 경과관찰 | 치료결과1)(어지럼증) | 치료결과 (청력) | 치료결과 (이명) |
|---|---|---|---|---|---|---|---|---|---|
| 고실 내 lidocaine 주입술과 고실 내 스테로이드 주입술의 비교 | |||||||||
| [20] | Sakata et al. (1986), Japan | Lid | NA | NA | NA | 효과있다: 42/47귀 | 변화없다 | 효과있다: 36/57귀 | |
| Dex | 효과있다: 21/21귀 | 변화없다 | 효과있다: 26/42귀 | ||||||
| [10] | Ito et al (1991), Japan | 총 136명 - Lid: 75명 - Dex: 61명 | 4% Lid + Dex 2 mg (0.5 mL) | 4 – 5회 | 3 – 4일 | NA | Class A – C of vertigo control: 57% (AAOO criteria, [1972]) | NA | 이명효과 Excellent 39%, good 22% |
| Dex 2 mg (0.5 mL) | 4 - 5회 | 1 – 2일 | NA | Class A – C of vertigo control: 80% (AAOO criteria [1972]) | 저음역 청력저하에서 더 효과적, 심고도난청에는 poor | 이명효과 Excellent 45%, good 29% | |||
| 고실 내 gentamicin 주입술과 고실 내 스테로이드 주입술의 비교 | |||||||||
| [30] | Patel et al (2016), UK | 총 60명 - MP: 30명 - Gen: 30명 | MP 62.5 mg/mL | 2회 | 2주 | 24개월 | 어지럼 없다: 20 | PTA 평균 2.1 감소 | THI 평균 19.8 감소 |
| Gen 40 mg/mL | 어지럼 없다: 19 | PTA 평균 6.4 감소 | THI 평균 21.3 감소 | ||||||
| [34] | Harcourt et al (2019), UK | 총 46명 - MP: 22명 - Gen: 24명 | MP 62.5 mg/mL | 2회 | 2주 | 6, 24, > 48개월 (평균 70.8개월) | 급성 어지럼발작 횟수 감소(16.2 → 0.8) | NA | 두 그룹 모두 THI 평균이 치료 24개월째에 감소했다가 이후 48개월 이상의 장기간 경과관찰에서 약간 상승 |
| Gen 40 mg/mL | 급성 어지럼발작 횟수 감소(18.3 → 1.0 # 장기간 경과 관찰에서 두 그룹 간에 차이 없이 치료효과 유지됨 | NA | |||||||
| [38] | Gabra et al. (2013), Canada | 총 89명 - MP: 42명 - Gen: 47명 | MP 62.5 mg/mL | 3회 | 1주 | 6 – 12개월 | Class A in vertigo control: 48.1% | PTA 평균 7.6 증가 | Tinnitus control: 68% |
| Gen 26.7 mg/mL | Class A in vertigo control: 82.9% # 두 그룹 간 뚜렷한 차이 보임(p=0.004) | PTA 평균 6.6 감소 # 두 그룹 간 뚜렷한 차이 없음 (p=0.06) | Tinnitus control: 27.3% # 두 그룹 간 뚜렷한 차이 보임(p=0.002) | ||||||
| [29] | Casani et al. (2012), Italy | 총 60명 - Dex: 28명 - Gen: 32명 | Dex 4 mg/mL | 3회 | 3일 | 24개월 | Class A – B in vertigo control: 17 (60.8%) | PTA 평균 0.5 감소 | NA |
| Gen 27.6 mg/mL - 1회: 19명 - 2회: 13명 | 1 - 2회 | >20일 | Class A – B in vertigo control: 30 (93.8%) # 두 그룹 간 뚜렷한 차이 보임(p<0.01) | PTA 평균 5.8 증가 # 두 그룹 간 의미있는 차이 없음 (p>0.05) | NA | ||||
| 고실 내 스테로이드 주입술과 Placebo 및 보존적치료의 비교 | |||||||||
| [39] | Garduño- Anaya et al. (2005), Mexico | 총 18명 - T: 11명 - C: 7명 | T: Dex 4 mg/mL | 5회 | 1일 | 24개월 | Class A–B in vertigo control: 11 | PTA 평균 2.2 감소 | THI 평균 37.8 감소 |
| C: Pla | Class A-B in vertigo control: 4 | PTA 평균 0.5 감소 | THI 평균 41.2 감소 | ||||||
| [56] | Silverstein et al (1998), USA | 총 20명 | T: Dex | 3회 | NA | NA | Caloric test상 변화 없음 | PTA 평균 유의미한 변화 없음 | THI 평균 유의미한 변화 없음 |
| C: Pla | Caloric test상 변화 없음 | PTA 평균 유의미한 변화 없음 | THI 평균 유의미한 변화 없음 | ||||||
| [9] | Paragache et al. (2005), India | 총 40명 - T: 20명 - C: 20명 | T: Dex (0.20 mg/ mL, 5 방울)을 VTI통해 3개월간 점적 | - | - | 1, 3, 6개월 | Vertigo control: 9명 (45%) (Sakata’s criteria) | PTA 평균 유의미한 변화 없음 | 이명 완전 소실 2(10%), 이명 호전 12명(60%) |
| C: 보존적 치료 ± 급성기 증상조절약물 or betahistine 유지치료 | 1, 3, 6개월 | Vertigo control: 8명(40%) # T, C 모두에서 경과관찰 길어질수록 감소하는 양상 | 이명 완전 소실 3명(15%), 이명 호전 10명(50%) | ||||||
| [8] | Albu et al. (2015), Italy | 총 59명 - T: 30명 - C: 29명 | T: IT Dex (4 mg/mL, 1 mL)+ PO pla | 3회 | 1일 | 12개월 | Class A-B in vertigo control: 21 (66.6%) | PTA 평균 유의미한 변화 없음 | THI 평균 5.1 감소 |
| C: IT NS (1 mL) + PO Bet (144 mg/day) | Class A-B in vertigo control: 17 (58%) | THI 평균 4.9 감소 | |||||||
| [27] | Molnár et al. (2021), Hungary | 총 70명 - Bet + Dex: 35명 - Bet: 35명 | IT Dex 4 mg/mL + PO Bet 72-144 mg | 5회 | 1일 | 54.4개월 (13.76-68.17) | 두 그룹 간에 급성 어지럼 발작의 발생(occurrence) 및 빈도(frequency)에 유의미한 차이 없음 | NA | NA |
| PO Bet 72-119.6 mg | 48.87개월 (12.43- 61.3) | NA | NA | ||||||
| 고실 내 스테로이드 주입술 후 치료결과 분석 | |||||||||
| [26] | Pradhan et al. (2017), India | 총 30명 | Dex 4 mg/mL, 0.3-0.5 mL | 3회 | 1주 | 27개월 (3-48) | DHI 평균 감소 (p=0.49) 어지럼 없는 환자수 경과관찰 길어질수록 감소 | PTA 평균 증가 (p=0.25) | |
| [40] | Memari et al. (2014), Iran | 총 100명 | Dex 4 mg/mL, 0.4-0.5 mL | 3회 | 1주 | 3주 | NA | PTA 평균 7 감소 (p<0.05) | THI 평균 9 감소 (p<0.05) |
| [42] | She et al. (2015), China & USA | 총 17명 | MP 20 mg, 0.5 mL | 10회 | 1일 | 6 > 24개월 | Class A-B in vertigo control: 94%(6개월), 81%(24개월), 70%(36개월) | PTA 평균이 6개월 후 감소, 2년후 다시 증가. 이러한 변화는 청력 stage에는 영향 없음 | 3명에서 호전, 2명은 2년 후에도 호전된 상태 |
| [43] | Masoumi et al. (2017), Iran | 총 69명 - Dex: 36명 - MP: 33명 | Dex 4 mg/dL | 3회 | 1주 | 1-6개월 | Class A-B in vertigo control에서 두 그룹 간 차이 없음 | PTA는 Dex보다 MP를 주입한 군에서 더 향상됨 (p=0.006) | NA |
| MP 40 mg/dL | |||||||||
| [41] | Jumaily et al. (2017), USA | 총 18명 | Tri 40 mg/mL ± Dex 4 or 10 mg/mL | 4.8회 (2-19) | NA | 41개월 (1-101) | Vertigo control: 74.7% | 청력변화 불명확(40%는 변화없음, 40%는 저하, 20%는 향상) | NA |
| [54] | Yu et al. (2020), China | 총 201명 - T1: 75명 - T2: 73명 - C: 53명 | -T1: IT Dex, 4회 | 4회 | 1주 | 3개월 | DHI 점수는 T1, T2에서 C에 비해 감소 (p<0.01), 메니에르병 후기보다 초기에 더 감소(p<0.05), Caloric test canal paresis value 초기 T1, T2에서 감소, VEMP에서는 유의미한 차이 없음 | NA | NA |
| -T2: IT Dex, 8회 | 8회 | 1주 | |||||||
| - C: 생활습관교정 및 약물치료 | |||||||||
| [48] | Beyea et al. (2017), Canada | 총 106명 | T1: 10분 간격으로 Dex 10 mg/mL, 2회 주입 | 1회 | 35개월 (29일- 7.3년) | NA | 치료전과 가장 마지막 PTA상 평균 8.27 증가(p<0.0001), T1, T2간에는 PTA 차이 없음 | NA | |
| T2: 위와 같음 | 4-29회 | 1주 | NA | NA | |||||
| [49] | Leng et al. (2016), China | 총 51명 | IT Dex 5 mg/mL - single: 37명 - multiple: 11명 | 1회 | 26개월 (14-77) | Class A in vertigo control이 1회 주입보다 2회 이상 주입시에 15.7%씩 감소 | PTA 변화 없음 (p>0.05) | NA | |
| 2-4회 | 6-50개월 | NA | |||||||
메니에르병에서 고실 내 주입술을 통해 dexamethasone을 적용한 경우26,40)와 methylprednisolone을 적용한 경우42)가 있으며, 둘 모두 어지럼 혹은 청력 호전을 보고하였으며, 둘 사이에 일관적인 차이는 없었다. Dexamethasone과 triamcinolone을 이용한 연구도 있으나, 두 가지 약제를 병행한 경우가 있고, 대상환자수가 적어 약제 간의 비교는 불가능했다.41) Masoumi 등의 연구에서는 methylprednisolone 40 mg/dL를 주 3회 주입한 그룹과 dexamethasone 4 mg/dL를 주 2회 주입한 그룹으로 나누어 어지럼증 및 청력 면에서 치료 결과를 비교하였다.43) 결과적으로, 두 약제는 어지럼증의 조절에 있어서는 통계적으로 유의미한 차이를 보이지 않았으나, 청력 개선에 있어서는 methylprednisolone을 사용한 그룹에서 더 의미있는 호전을 보였다.
약제에 따라, 치료 효과에서는 명확한 차이를 보이지 않았으나, 합병증에서는 차이가 뚜렷했다. Dexamethasone과 triamcinolone을 적용한 연구에서 통증을 호소한 환자는 없었던 반면,41) methylprednisolone을 고실 내 주입한 연구에서는 환자들이 주입 측 귀 및 인두부의 타는듯한 통증이나 불편감을 호소하는 경우가 있었다.42,44) Triamcinolone을 적용한 경우에서 높은 확률로 고막천공이 발생했는데,41) triamcinolone이 현탁액 형태로 중이 공간에 주입되면서 약제 입자(steroid particle)가 고막 내면을 덮거나 막아 자연회복을 방해했을 가능성이 있다. 그러나 반복적으로 여러 번 고실 내 주입술을 시행하였으므로, triamcinolone 약제 자체의 영향에 대해서는 추가적인 연구가 필요하다.
Triamcinolone과 dexamethasone은 매우 유사한 분자구조를 가지고 있지만, 임상에서 주로 용액 형태인 dexamethasone에 비해 triamcinolone은 주로 하이드로겔이나 현탁액 형태이므로 보다 오래 머물면서 지속적 효과(sustained release)를 보일 것으로 생각되며,45) 실제로 안과영역에서는 이러한 효과로 사용되고 있다.46) 그러나 실제로 고실 내 주입했을 때 스테로이드 약제의 형태(용액 또는 현탁액)에 따라 그 효과에서 차이가 있는지는 불확실하다.
고실 내 스테로이드 주입술에서, 주입한 약물의 용량(volume)은 명시되어 있는 경우와 명시되지 않은 경우를 통틀어 약 0.5 mL(중이 공간을 채울 정도의 용량)로 추정된다.
Parnes는 고실 내로 약제를 얼마나 많이 주입하는지 보다는 주입용액 내 약물의 농도와 약물이 정원창 막과 접촉하는 시간이 더 중요하다고 말한다.21) 실제적으로 병원에 온 바쁜 외래환자가 고실 내 주입술을 시행 후 자세를 유지하는 시간은 길어야 20-25분 정도에 불과하므로, 같은 용량이라면 더 높은 농도로 불편감 없이 투여 가능한 약제가 선호될 것이다.
현재 국내에서 생산/유통되는 dexamethasone disodium phosphate가 1 amp 기준으로 5 mg/mL이고, Triamcinolone acetonide가 1 vial 기준 40 mg/mL, methylprednisolone sodium succinate가 1 vial 기준으로 40 mg, 125 mg 혹은 500 mg가 있다. Dexamethasone은 그 이상의 고농도를 적용하기 어려우나, methylprednisolone 및 triamcinolone의 경우 다양한 농도로 적용 가능하다.
같은 약제에서 농도에 따른 차이를 비교한 연구는 없으나, dexamethasone 4 mg/mL와 methylprednisolone 40 mg/mL를 비교하였다.43) 두 약제가 역가에 따른 동일용량은 아니었으나, 치료결과에서 차이를 보이지 않았다.
메니에르병에서 고실 내 스테로이드 주입술의 효과에 대한 대부분의 연구에서, 고실 내 주입술을 반복적으로 여러 번 시행하였다(Table 2). 주입 횟수는 2회에서 7회 이상으로 매우 다양하며, 주입 간격 또한 1일에서 2주로 매우 다양하다.
Plontke 그룹의 연구에서 고실 내 스테로이드 주입술 이후 와우 내 농도변화를 확인하였는데, 여러 번 주입하거나, 지속적으로 주입한 경우에서 와우 정점부(cochlear apex)에서 더 높은 농도가 확인되었다.47,11)
고실 내 약물 주입술의 시행 횟수에 따른 실제적 치료효과를 비교연구한 논문에서, 일회 시행한 경우와 여러 차례 시행한 경우 사이에 청력은 유의미한 차이를 보이지 않았으나, 어지럼 증상의 조절에서는 유의미한 차이를 보였다.48,49) 같은 methylprednisolone 62.5 mg/mL를 1주 이상의 간격으로 주입한 경우29,30,34,38)와 20 mg을 매일 10일간 주입한 경우42)를 비교해 보면, 어지럼 증상이 조절되는 비율이 후자의 경우에서 뚜렷이 높은 것을 볼 수 있다. She 등은 고실 내로 methylprednisolone을 주입하고 2시간 후에 perilymph에서 최대 농도를 이룬 뒤 6시간 정도를 고농도를 유지하고 24시간 후 점진적으로 감소하므로,21) 매일 고농도를 주입하는 것이 필요하다고 기술하였다.42)
다만, 고막천자 혹은 환기관을 통해 여러 번 주입한 경우에서 1.6%-7.3%의 확률로 영구적 고막천공이 확인되었고,50-52) 그 외에 중이염, 청력 저하 등이 보고되기도 하였다. 다만, 이러한 합병증의 발생에는 주입술의 횟수뿐 아니라, 스테로이드 주입방법(needle을 이용하여 고막천자 후 주입 혹은 환기관을 통한 주입 등) 또한 영향을 줄 것으로 추정되며,53) 고막 천자를 시행한 부위와는 무관하다.52)
메니에르병이 진행되면서 내이에 영구적인 손상이 발생하기 전, 질환을 진단받고 고실 내 스테로이드 주입술을 받을 때까지의 시간이 짧을수록 효과적이라는 여러 연구들이 있다.10,16,54) 이에 따라 고실 내 스테로이드 주입술을 시행한 후 증상의 개선은 주로 초기(early stage) 메니에르병 환자의 경우에서 일어나며, 영구적 손상이 발생한 후기(late stage) 메니에르병에서는 효과를 보기 어렵다고 추측해볼 수 있다.
고실 내 스테로이드 주입술이 메니에르병의 모든 증상 조절에 효과적인지에 대해서는 아직 의견이 분분하다. 어지럼증뿐 아니라, 이명이나 청력저하와 같은 청각증상에도 효과적이라고 보고한 연구도 있으나,10,40,55) 반대로 청각증상에서 의미있는 효과는 없고, 주로 전정증상의 조절에 효과적이라고 보고한 연구들도 있다.25,49,56) 하루 144 mg 이상의 고용량 Betahistine 치료와 비교했을 때 큰 차이가 없다고 보고한 연구도 있다.8)
2021년 현재, 메니에르병에서 고실 내 스테로이드 주입술의 효과에 대해서는 의견이 분분한 상태이다. 그래서 고실 내 스테로이드 주입술의 적응증 및 프로토콜 등의 표준화가 이루어지지 않아, 현재 시행된 고실 내 스테로이드 주입술에 대한 연구들은 치료를 시행한 대상 환자군, 고실 내 스테로이드 주입술의 시행시기 및 횟수, 사용한 스테로이드 약제의 종류 및 형태 등이 매우 다양하다. 뿐만 아니라, 고실 내 스테로이드 치료의 효과를 평가하는 방법, 경과관찰의 간격과 기간 또한 매우 다양하다. 향후 연구에서는 보다 객관적인 결과를 도출하기 위해서 대상 환자군의 선정 기준과 치료 적응증 및 프로토콜 등을 통일하여 전향적, 무작위 대조군 연구를 통해 치료결과를 비교 분석하는 것이 필요하다.
결론
고실 내 스테로이드 주입술은 메니에르병으로 확진된 환자가 다른 보존적 치료에도 효과가 없는 경우, 수술이나 고실 내 겐타마이신 주입술과 같은 치료를 시행하기 전에, 그와 유사한 효과를 낼 수 있는 구제적 치료법으로서 선택해볼 수 있다. 내이에 영구적 손상이 발생하기 전, 메니에르병 초기에 고실 내 주입술을 시행하는 것이 청각 및 전정증상의 조절에 효과적일 수 있다. 스테로이드 약제간의 차이가 명확히 확인된 바는 없으며, 주입 용량보다는 주입된 약물의 농도와 중이 공간에서 정원창에 접촉하는 시간이 길수록 효과적으로 전달될 것으로 생각된다. 이러한 이유로, 일회성보다는 여러 차례 주입술을 시행하는 것이 선호된다. 그러나, 실제적으로 주입횟수와 비례하여 효과의 차이를 보이지는 않았고, 오히려 고막 천공과 같은 합병증 발생의 위험이 증가할 수 있으므로, 국소소견 및 증상을 면밀히 경과 관찰하면서 진행해야 한다.
여러 연구에서 다양한 약제와 다양한 방법으로 고실 내 주입술을 시행하고 있어, 고실 내 스테로이드 주입술이 메니에르병에서 얼마나 효용을 보이는지 아직 결론짓기는 어렵다. 향후 연구에서 보다 통일된 조건 및 기준 하에, 약제의 종류나 농도, 주입용량, 지속시간 등에 따라 결과를 분석하는 것이 필요하다.






